


流式细胞术广泛运用于从基础研究到临床实践的各个方面,用于基于细胞层面不同亚群生物指标、分化状态、活化、增殖经历过程。免疫疗法的重点是通过抗体与不同免疫细胞亚群上的受体结合,并根据所其产生的激活或抑制功能现 象调整临床免疫反应策略。受体占位生物分析常用的检测技术为流式细胞技术。在免疫疗法中,RO作为药效学(PD)的生物指标,与药代动力学(PK)相结合,指导临床治疗应用。
受体占位检测,顾名思义是药物对细胞 表面靶受体占有情况的检测。在抗体药物对细胞靶向治疗的过程中,受体占位是一种重要的药效动力学生物指标。 R O 占有过低,可能会起不到治疗效果;而如果长期 RO 占有过饱和状态,会有过度结合,导致一定的副作用或者毒性。
受体占位在细胞靶向治疗生物药临床研究各个阶段都具有重要作用。
在临床I期,受体占位有助于药物从动物到人的靶点确证,考虑种属差异,受体表达丰度差异等因素,通常临床试验受体占位检测方法需要重新优化。
临床II期,受体占位确证药物浓度、受体结合、免疫原性抗药抗体( ADA) 和药效的关系。帮助确定临床有效剂量,指导决策。
临床III期,受体占位辅助确定抗体药物的群体PK特征。确定年龄、性别、体质量等协变量是否对生物药作用机制有影响。上市后,受体占位用于开发新适应症或下一代治疗剂的比较。特别是在早期临床,受体占位有助于建立基于最小生物学效应水平MABLE 的临床前到临床的准确首次人体剂量优化模型 [1] 。
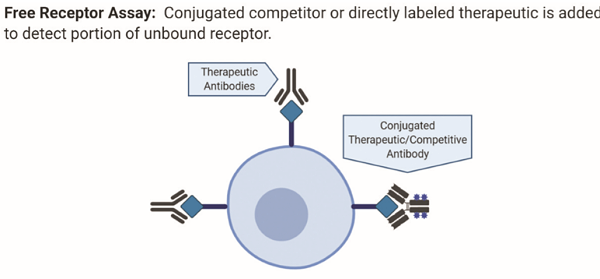
图1:自由检测法原理
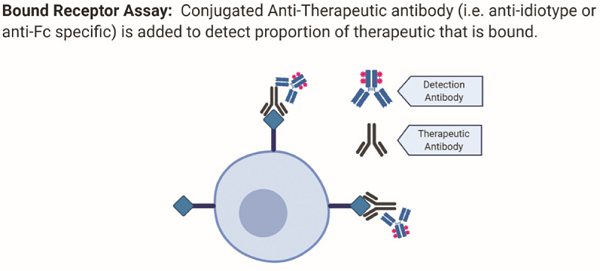
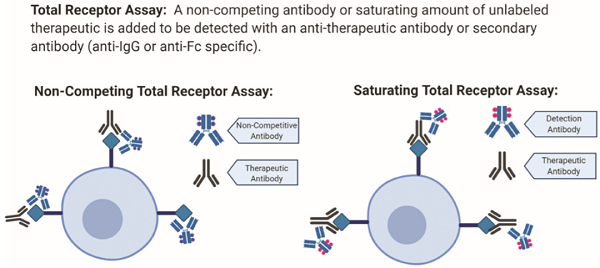
图3:总受体检测法原理
ROA(RO Assay)设计之前考虑的因素:
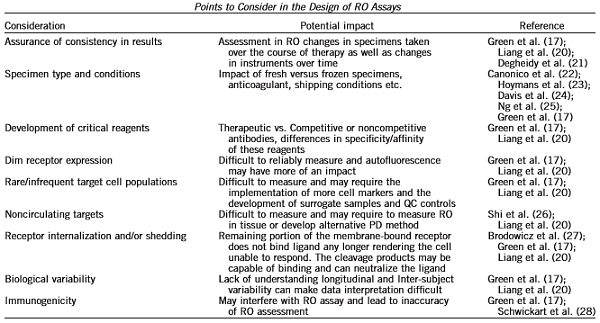
表1:ROA考虑因素
[ 1 ] 中国临床药理学与治疗学 , 2020 Jan; 25
[2] Alessandra Audia, Gregory Bannish, Rachel Bunting and Chelsea Riveley (2022). Flow cytometry and receptor occupancy in immune-oncology. Expert opinion on Biological therapy. Vol.22, NO,1, 87-94.
[3] Jennifer J.Stewart, Cherie I.Green, Nicholas Jones, Yuanxin Xu, et al.(2016). Role of Receptor Occupancy Assays by Flow Cytometry in Drug Development. Cytometry B: (Clinical Cytometry) 90B:110-116.
本文标签: 药物临床前服务 药物临床前研发服务 靶向药伴随诊断 核酸检测多少钱 生物标志物分析