


近日,迈杰转化医学宣布其自主研发的Claudin18.2、PD-L1、MMR、MSI、c-MET等5款实体肿瘤伴随诊断产品,以及MPN四联检、血液肿瘤Ig/BCR重排MRD监测、BCR-ABL定量监测等3款血液肿瘤产品获得了欧盟CE认证, 分别为:
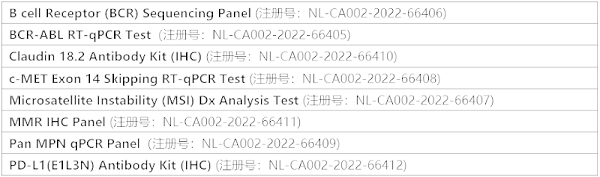
8款产品的获批意味着迈杰转化医学在全球化布局道路上迈出了重要的一步,有助于提升公司在国际市场的知名度与品牌效应。
在伴随诊断和体外诊断产品研发方面,迈杰转化医学在实体瘤与血液肿瘤产品赛道双布局,涵盖了IHC、PCR、NGS等主流技术平台,以多元化、临床应用为导向的产品加速领跑诊断行业。公司拥有国际一流的产品开发团队及完善的产品研发流程,目前在国内已经上市了 JAK2-V617F基因突变检测试剂盒(国内首款)、c-MET抗体检测试剂、dMMR抗体检测试剂、Claudin18.2抗体检测试剂、pan-TRK抗体检测试剂等多款试剂 , PD-L1抗体检测试剂 注册申报正在稳步推进,多款产品已经应用于临床、ICL以及创新药企的伴随诊断。
与此同时,迈杰转化医学正积极推动多款伴随诊断和体外诊断产品的研发,临床试验、全球注册以及商业化布局。除CE认证外,FDA注册申报也快速推进中,未来将有更多的产品全球上市,用于伴随/辅助诊断、用药指导、预后监测等,致力于精准医疗。
本文标签: 药物临床前服务 药物临床前研发服务 靶向药伴随诊断 核酸检测多少钱 生物标志物分析