


近期,由中国医学科学院肿瘤医院(国家癌症中心)和复旦大学等院所联合研究4种不同克隆号PD-L1抗体免疫组化(Immunohistochemistry,IHC)检测食管鳞状细胞癌患者PD-L1表达的一致性结果在《Journal of the National Cancer Center》发表,结果显示4种国产抗体(E1L3N XP,MXR006, BP6099,CST E1L3N)与PD-L1 22C3在食管鳞癌中分析性能相关性良好,临床诊断性能一致性较好。证明了这些抗体,尤其是E1L3N与22C3抗体具有潜在互换性。
迈杰医学PD-L1检测试剂盒(免疫组织化学法)(商品名:迈谱康;克隆号:E1L3N), 于2022年9月由国家药品监督管理局(NMPA)批准上市作为非小细胞肺癌的伴随诊断试剂,迈杰医学多适应症扩展研究中显示迈谱康与22C3在食管鳞癌总符合率为95.0%。这项研究的结果夯实了E1L3N与22C3可互换性的结论,拓展了迈谱康的适应症范围,也为食管鳞状细胞癌临床病理诊断及检测提供了更灵敏和更精准的试剂选择。

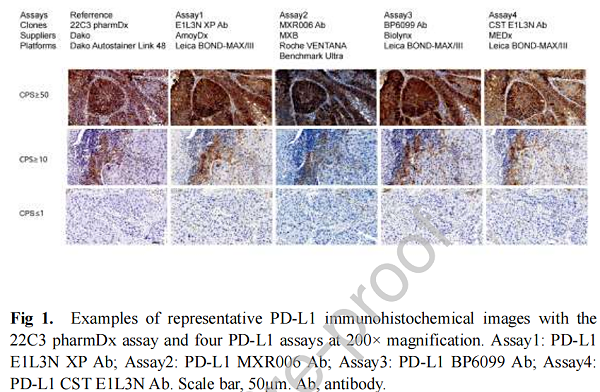
预测肿瘤免疫治疗反应主要依赖于程序性死亡配体1(PD-L1)免疫组化(IHC)状态,并且22C3 pharmDx检测试剂盒已经被批准适用于食管鳞状细胞癌(ESCC)。但是,该检测试剂盒的广泛使用因其适用性而受到限制。因此,需要寻找替代的PD-L1检测试剂盒。我们旨在研究四种PD-L1检测试剂盒的分析性能和临床诊断性能,并比较其与22C3 pharmDx检测试剂盒的一致性。
1、四种PD-L1测试试剂盒的分析性能比较
PD-L1染色测定CPS和TPS
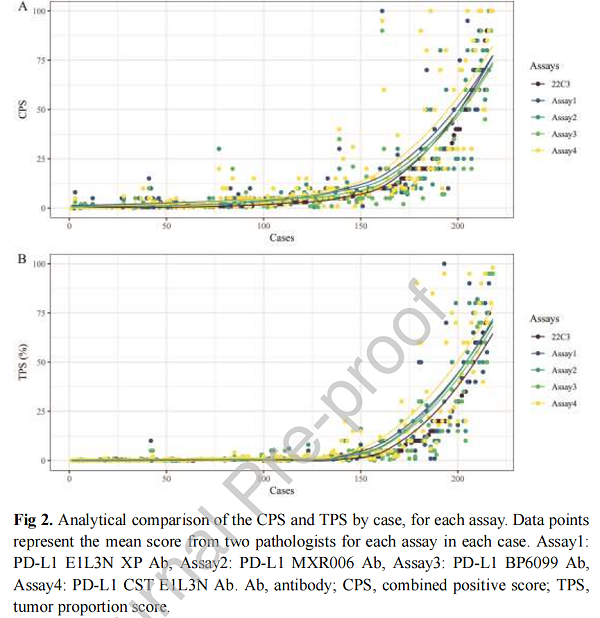
218例患者的CPS和TPS检测结果如图2所示:
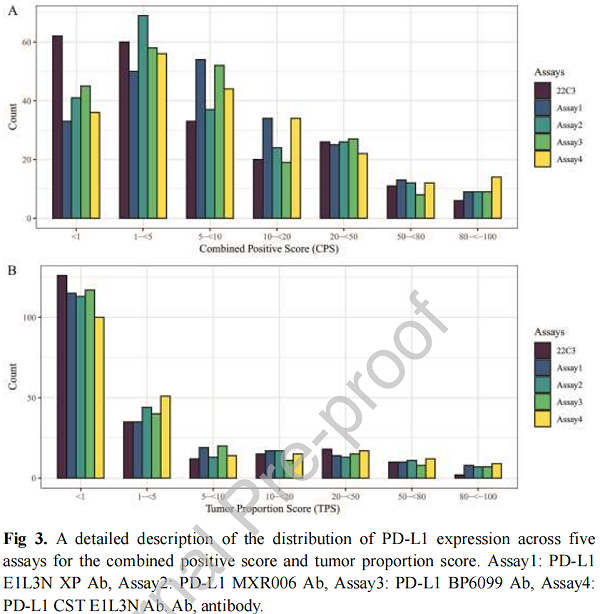
根据CPS和TPS成对比较PD-L1染色
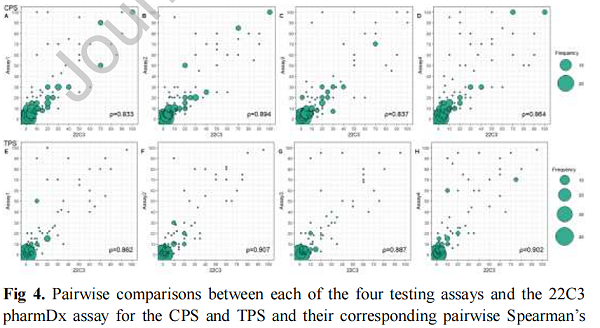

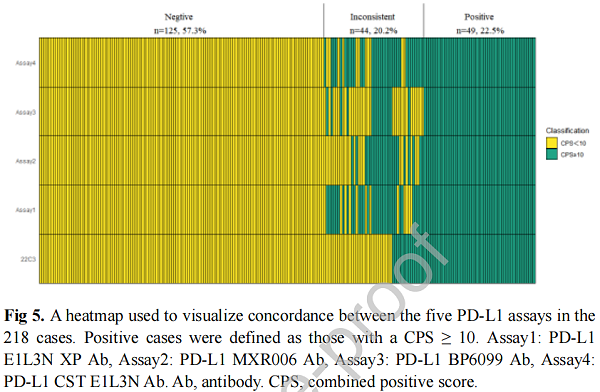
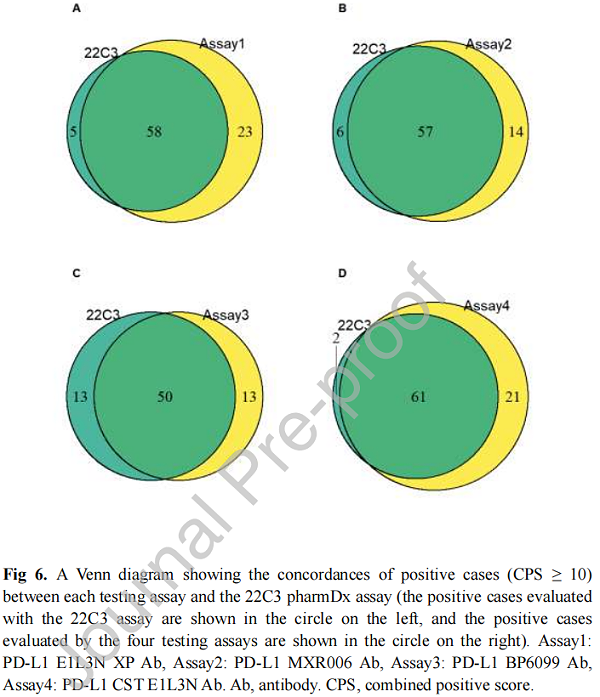
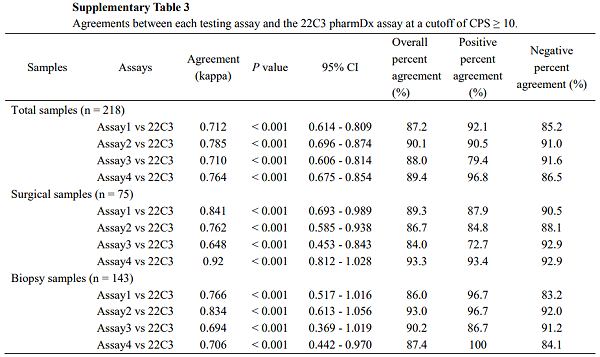
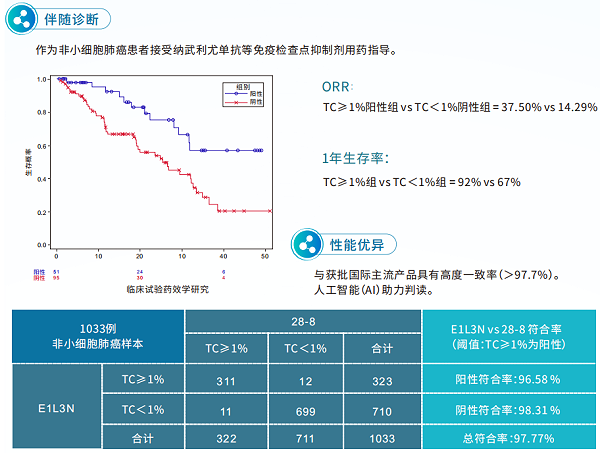
迈杰医学拥有自研产品“迈谱康”——PD-L1检测试剂盒(免疫组织化学法)(注册证编号:国械注准20223401300),该产品为NMPA-Ⅲ类CE-IVD,可用于抗PD-(L)1抑制剂伴随诊断。
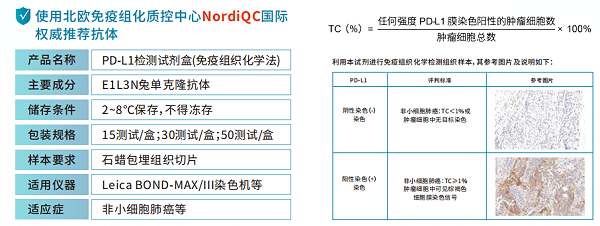
4.适⽤平台⼴,适⽤于Leica、Ventana、国产等多平台。

本文标签: 药物临床前服务 药物临床前研发服务 靶向药伴随诊断 核酸检测多少钱 生物标志物分析